Eliisabeth Kuldmaa, Indrek Koppel
Eelmises numbris andsime ülevaate gliiast ehk nendest närvisüsteemirakkudest, mis ei ole neuronid. Viimastel aastakümnetel on neurobioloogid pööranud nendele rakutüüpidele üha suuremat tähelepanu. Tõuke on andnud ennekõike uurimisviiside tehnoloogilised uuendused, mis võimaldavad paremini aru saada, millises koes üks või teine huvipakkuv protsess aset leiab. Kuna eri tüüpi rakud paiknevad lootusetult läbisegi, kulgevad protsessid korraga mitmes rakutüübis või on nende omavahelise suhtlemise tulemus. See asjaolu teeb uuringud raskemaks, kuid ka põnevamaks.
Ajapikku on saanud selgemaks, milliseid ülesandeid eri tüüpi gliiarakud täidavad. Võtame vaatluse alla kolme ajus leiduva gliiarakkude põhitüübi – astrotsüütide, mikrogliia ja oligodendrotsüütide otstarbe. Ühtlasi käsitleme lähemalt oligodendrotsüütide eellasrakke, mida praegu peetakse samuti gliiarakkude tüübiks.
Astrotsüüdid, mitmekülgsed abimehed
Kaks kõige arvukamat aju gliiarakkude tüüpi on astrotsüüdid ja oligodendrotsüüdid. Alustame astrotsüütidest. Need on saanud nime tähekujulise välimuse järgi: sellisena paistsid nad algul mikroskoobis. Astrotsüüdid on üks esimesi gliiarakutüüpe, mida on 19. sajandi lõpus histoloogiliste värvingute alusel põhjalikult kirjeldanud Santiago Ramón y Cajal, rakulise neuroteaduse isa.
Astrotsüüdid kuuluvad paremini uuritud gliiarakkude hulka, neil on kirjeldatud mitu olulist ülesannet. Nad aitavad tagada sünapside ehk neuronitevaheliste kontaktide toimimise (sünaptiline homöostaas), osalevad organismi arengus sünapside loomisel, muudavad sünaptilise närviimpulsi ülekande tugevust, loovad vere ja aju barjääri (vereaju ehk hematoentsefaalne barjäär on rakuline tõkend, mis pakub ajule erikaitset kahjulike ainete ja haigustekitajate eest), reguleerivad ajus verevoolu, eemaldavad ajust jääkaineid ja koguvad neid lümfisüsteemi ning toetavad neuronite ainevahetust.
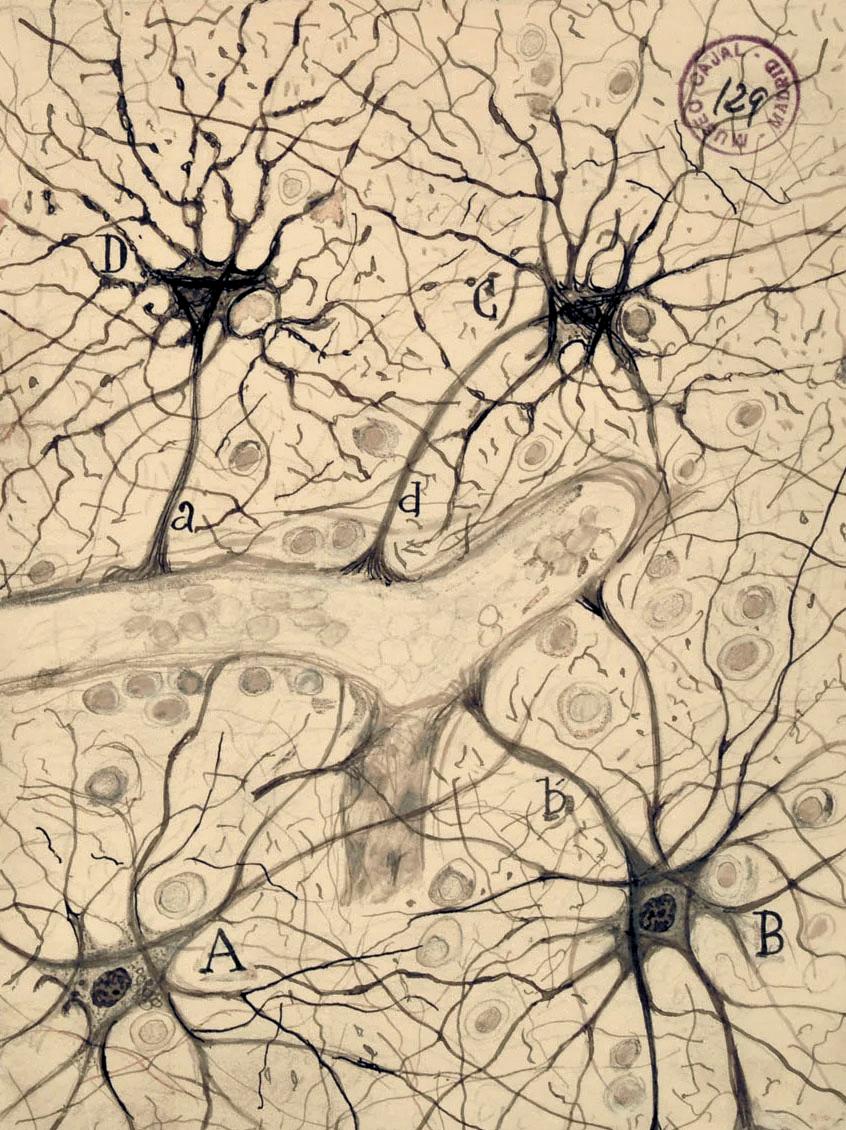
Neuroteaduse loojaks peetava Santiago Ramón y Cajali 19. sajandi lõpust pärit joonistus astrotsüütidest, mis ümbritsevad veresoont ajukoore valgeaines. CAJAL INSTITUTE, CAJAL LEGACY, CSIC
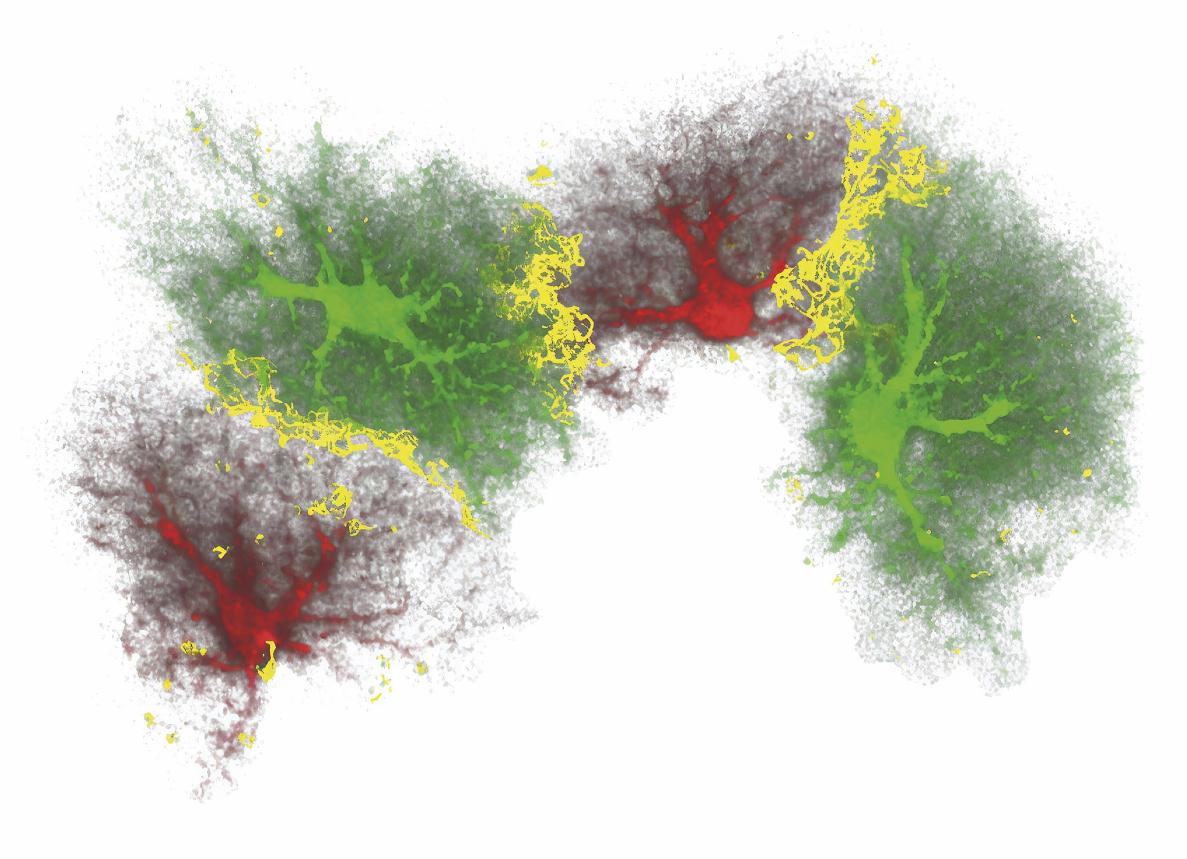
Ajakohane mikrofotograafiline 3D-rekonstruktsioon atsrotsüütidest. Astrotsüüdid on tehtud nähtavaks punase ja rohelise värviga ning tühimikud ja ühenduskohtadevahelised kommunikatsioonipiirkonnad kollasega. ALLIKAS: WILHELMSSON ET AL., 2006, PNAS
Kuna astrotsüütidel on nii palju tähtsaid ülesandeid, on neid seostatud paljude närvisüsteemi haiguslike protsessidega. Neist tuntuim ja levinuim on Alzheimeri tõbi, mida on muu hulgas seostatud astrotsüütide patoloogiatega. On uuritud Alzheimeri tõve patsientide ajusid surma järel ning märgatud astrotsüütide kuju (jämedamaks muutunud jätked) ja biokeemilise koostise muutusi. Teine väga selge vihje on apolipoproteiin E (APOE) valku kodeeriv geen. Hilise algusega Alzheimeri tõve kõige tugevamaid riskitegureid on mõningad mutatsioonid APOE-geenis. Selle geeni kodeeritud valk avaldub põhiliselt astrotsüütides, seetõttu on mutatsioonide põhjustatud molekulaarne viga suure tõenäosusega seotud just nende rakkudega.
Peale Alzheimeri tõve on leitud astrotsüütide seoseid depressiooni, skisofreenia ja teiste psühhiaatriliste häiretega. Haiguste täpsed mehhanismid ei ole teada, kuid tihti osutavad tõendite niidiotsad selgelt mõnele põletikulisele protsessile. Praegu ei tarvitata ühtegi spetsiifiliselt astrotsüütidele mõjuvat ravimit, aga tulevikus võib see teoks saada.
Vaatleme lähemalt mõnda tähtsamat astrotsüütide ülesannet. Esmalt käsitleme sünaptilist homöostaasi. Nagu neuronitel on ka astrotsüütidel palju peenikesi jätkeid. Raku keskpaigast ehk rakukehast lähtuvad jämedamat sorti jätked, mis harunevad järjest peenemaks. Harud lõpevad ülipeenikeste lõppjätketega, mis moodustavad sünapsi ümbritseva ehk perisünaptilise kapsli. Selle nn perisünaptilise jätke ülesanne on osaleda protsessis, mis taastab sünaptilise ülekande järel sünapsis paiknevate ioonide ja virgatsainete algkontsentratsioonid. Allpool oleval joonisel on see protsess esitatud aju kõige levinuma sünapsitüübi ehk glutamaatergilise sünapsi (kasutab virgatsainena aminohapet glutamaat) näitel. Niisugune sünaptiline majapidamistöö peab käima lakkamatult ja kui selles tuleb ette häireid, on tagajärjed halvad. Näiteks võimetus haarata astrotsüüdi lõppjätketesse piisavalt glutamaati toob kaasa glutamaatergiliste sünapside üleergastamise, mis võib ajendada epilepsia tekke. Päriliku epilepsia põhjustajana on teada mitu mutatsiooni astrotsüüdis toimetava glutamaadi transporteri geenis.
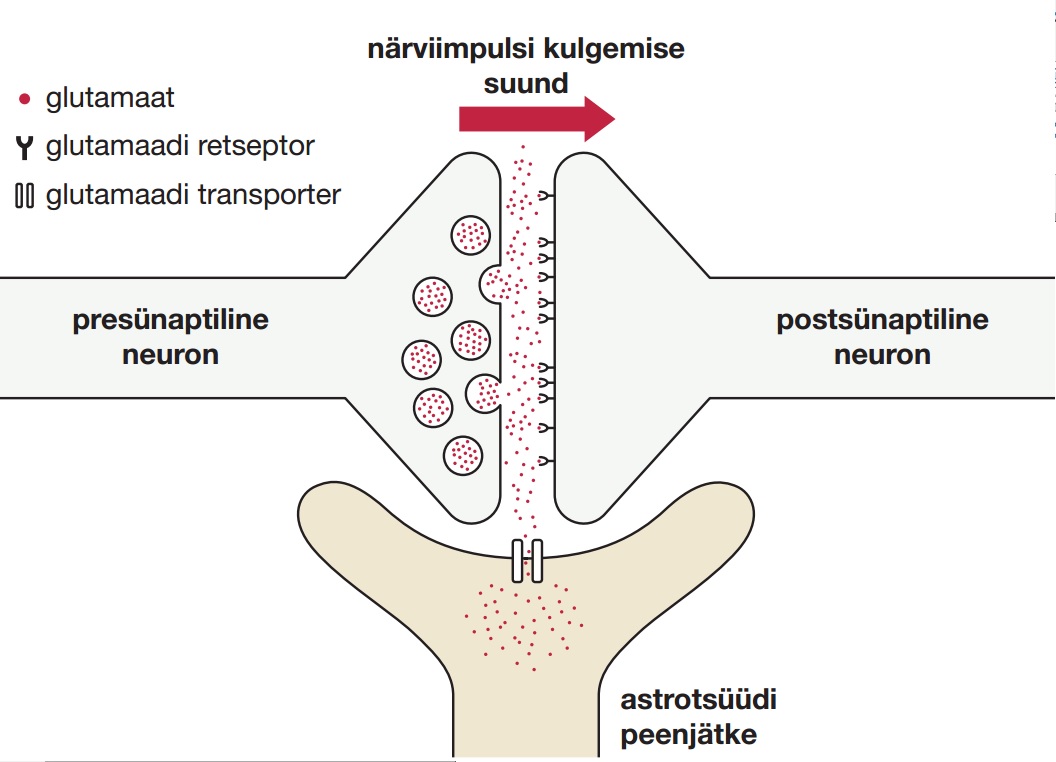
Kahest neuronist ja astrotsüüdist koosnev kolmeosaline sünaps: neuronite kokkupuutepunkt, kus närviimpulss kandub ühelt neuronilt teisele. Närviimpulss muundatakse elektrilisest keemiliseks virgatsainete kaudu. Joonisel on virgatsainena kujutatud glutamaati kui neist levinuimat. Glutamaat on koondunud presünaptilisel poolel põiekestesse, mis vabastavad impulsi käigus oma sisu sünaptilisse pilusse. Glutamaat seostub asjaomase retseptormolekuliga, mille tõttu muundatakse sünaptiline vastus uuesti elektriliseks. Viimastel aastakümnetel on välja kujunenud ettekujutus sünapsist kui kolme rakulise poolega struktuurist: peale kahe neuroni osalevad selles astrotsüüdid, mille jätked ümbritsevad sünapsi. Joonisel olevat astrotsüüdijätket tuleb kolmemõõtmelises ruumis ette kujutada nõnda, et ta ümbritseb neuronitevahelist kontakti. Üks astrotsüütide oluline roll sünaptilises ülekandes on eemaldada liigne glutamaat rakkudevahelisest ruumist. Niisugune mehhanism tagab selle, et sünaps on valmis vastu võtma uut impulssi ehk informatsiooni
Astrotsüüdid etendavad suurt osa ka teises võtmetähtsusega funktsioonis – aju energiavahetuses. Kehamassist ainult paar protsenti hõlmav aju kulutab kogunisti viiendiku meie omastatud energiast. Neuronite jagu on sellest energiast umbes 80–90%, sellest omakorda suurem osa tarvitatakse sünaptilistes infoülekannetes. Kummalisel kombel tarvitavad neuronid ainult umbes poole aju põhilisest energiaallikast glükoosist, ja teise poole kasutavad ära gliiarakud.
Ühtlasi on teada, et astrotsüütides paikneb suurem osa aju glükogeenist. Glükogeen ehk nn loomne tärklis on rakkudes glükoosi varuaine, mida rakendatakse siis, kui veres pole piisavalt glükoosi. Selline olukord energiamajanduses tekitab silmatorkava vastuolu: neuronid tarvitavad suurema osa energiast, aga ainult poole glükoosist. Kuidas see energiapuudujääk kaetakse?
Säärase ebakõla põhjal on oletatud, et gliiarakud pakuvad energiaablastele neuronitele tugiteenust, mis aitab nende elektrilisi protsesse sujuvalt käigus hoida. Oluline metaboliit, mille kaudu energiat üle kantakse, näib olevat piimhappe ioonvorm ehk laktaat, millega varustavad neuroneid põhiliselt astrotsüüdid. Neuronites kasutatakse laktaati energiarikka molekulina, mille varal saab sünteesida põhilist energeetilist valuutat – ATP-d. Mitme teadustöö põhjal on praeguseks kindlaks tehtud, et astrotsüütidelt neuronitele suunatud laktaaditranspordi häirumisel saab katsehiirtel kannatada pikaajaline mälu.
Mikrogliia – aju immuunrakud
Mikrogliia on gliiarakkude tüüp, mis on saanud nime suhteliselt väikeste rakukehade järgi, nad täidavad aju kohapealsete immuunrakkude ülesannet. Nende puhul torkab silma asjaolu, et nad paiknevad teiste närvisüsteemirakkudega võrreldes ajus väga ühtlaselt (erinevalt näiteks neuronitest, mis võivad asetseda üksteise kõrval tihedamalt või hõredamalt). Mikrogliia rakukehast ulatuvad välja pidevalt liikuvad jätked. Kui juuresoleval pildil olevatest rakkudest teha tunnipikkune video ning esitada see kiirendatult kümne sekundi vältel, võiks näha täiesti kepsakaid tantsuliigutusi. Nende liigutustega kobab mikrogliia oma ümbrust, et märgata patogeene või koekahjustusi. Kui need valvurrakud panevad tähele midagi kahtlast, annavad nad keemilisi signaalmolekule eritades teistele rakutüüpidele häiret ning võivad liikuda kahjustunud koepiirkonda, et see mikrokeskkond tervest koest isoleerida. Mikrogliia rakud on võimelised fagotsüteerima ehk alla kugistama end ümbritsevaid kahjulikke või ebavajalikke osakesi: rakuprügi, surnud rakke ja haigustekitajaid, mis võivad olla sattunud kesknärvisüsteemi.
Kuna ajukoes puudub võimalus kasutada antikehadel põhinevat immuunkaitset, on mikrogliia kanda eriti suur vastutus, et patogeenidele kiiresti reageerida ja nad kahjutuks teha. Mikrogliia neelamisvõimele on loodus leidnud ka teise kasuliku rakenduse sünapside kärpijana. Arengu käigus tekib igaks juhuks palju rohkem sünaptilisi kontakte, kui lõpuks kasutusele võetakse. Ülearuste sünapside eemaldamisel on olulisel kohal mikrogliiarakud, mis nad alla kugistavad, lagundavad ja võimaldavad selle käigus tekkinud molekulaarseid ehituskive taaskasutada, loomaks uusi rakulisi struktuure.